Cho m(g) Mg vào dung dịch chứa 0,1 mol AgNO3 và 0.25 mol Cu(NO3)2, sau một thời gian thu được 19,44g kết tủa và dung dịch X chứa 2 muối. Tách lấy kết tủa, thêm tiếp 8,4g bột sắt vào dd X, sau khi các phản ứng hoàn toàn, thu được 9,36g kết tủa. Giá trị của m là: A. B. C. D.
Thi đại học Hoá học Thi đại học - Hoá học Trang chủ Sách ID Khóa học miễn phí Luyện thi ĐGNL và ĐH 2023 Độ khó: Vận dụng
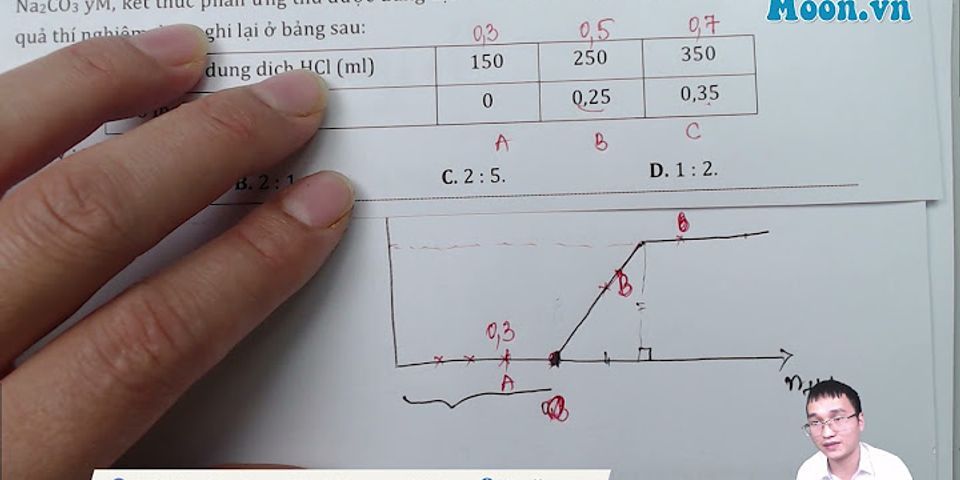
Cho m gam bột Mg vào dung dịch chứa 0,3 mol AgNO3 và 0,2 mol Fe(NO3)3, sau phản ứng thu được 38 gam chất rắn. Giá trị của m là:
   
Câu hỏi trên thuộc đề trắc nghiệm dưới đây ! Số câu hỏi: 1093 Đáp án: m=8,4 gam Giải thích các bước giải: Các phản ứng xảy ra: \(Mg + 2AgN{O_3}\xrightarrow{{}}Mg{(N{O_3})_2} + 2Ag\) \(Mg + 2Fe{(N{O_3})_3}\xrightarrow{{}}Mg{(N{O_3})_2} + 2Fe{(N{O_3})_2}\) \(Mg + Fe{(N{O_3})_2}\xrightarrow{{}}Mg{(N{O_3})_2} + Fe\) Nếu Ag thì rắn chỉ chứa 0,3 mol Ag. \( \to {m_{Ag}} = 0,3.108 = 32,4{\text{ gam}}\) Nếu Fe hết thì rắn chúa 0,3 mol Ag và 0,2 mol Fe. \( \to {m_{rắn}} = 0,3.108 + 0,2.56 = 43,6{\text{ gam > 38}}\) nên muối sắt dư Vậy rắn chứa 0,3 mol Ag và x mol Fe. \( \to {m_{Fe}} = 38 - 0,3.108 = 5,6{\text{ gam}} \to {{\text{n}}_{Fe}} = x = 0,1{\text{ mol}}\) \( \to {n_{Mg}} = \frac{1}{2}{n_{AgN{O_3}}} + \frac{1}{2}{n_{Fe{{(N{O_3})}_3}}} + {n_{Fe}} = \frac{{0,3}}{2} + \frac{{0,2}}{2} + 0,1 = 0,35{\text{ mol}}\) \(\to m = 0,35.24 = 8,4{\text{ gam}}\)
Bằng cách đăng ký, bạn đồng ý với Điều khoản sử dụng và Chính sách Bảo mật của chúng tôi. |